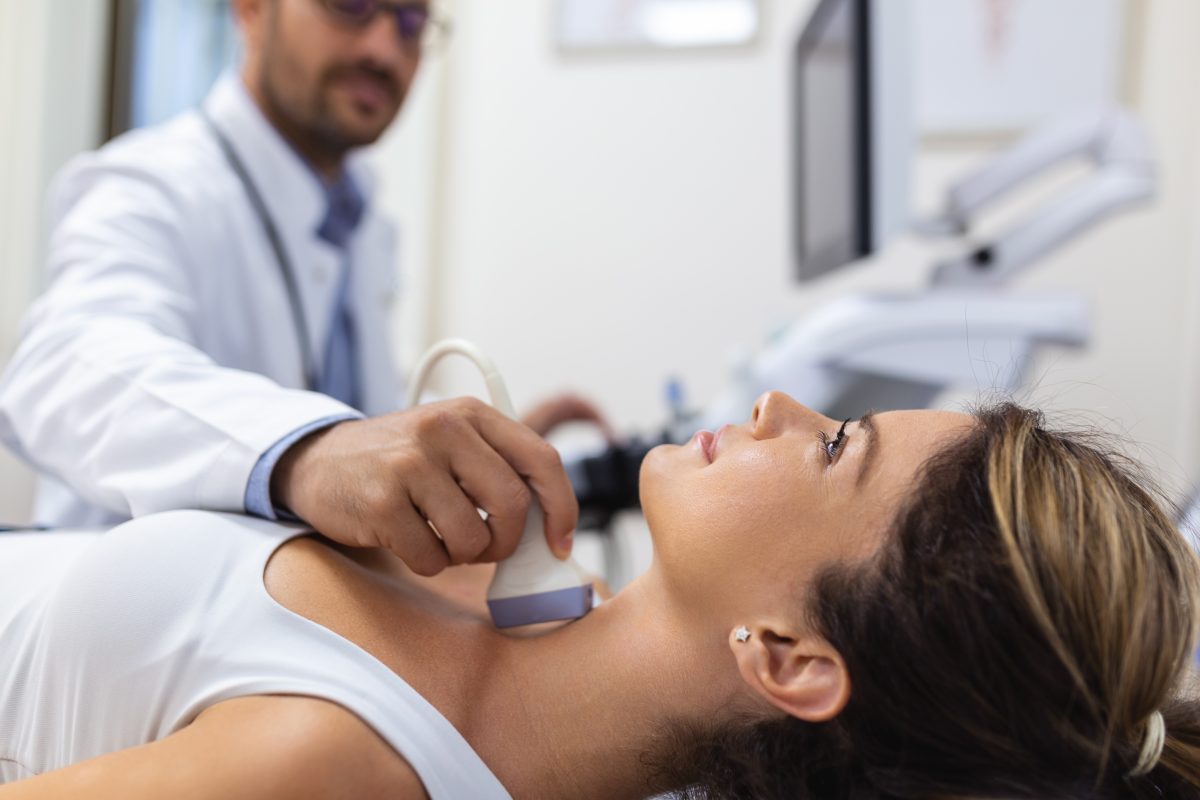
La biopsia tiroidea es un procedimiento destinado al análisis de los tejidos nodulares tiroideos y la extracción de una pequeña muestra celular, con el propósito de identificar la presencia de cáncer, infecciones u otros trastornos relacionados con la tiroides.
Tipos de biopsias tiroideas:
Un médico emplea una aguja delgada para acceder a la tiroides. Esta técnica de biopsia suele ser preferida por muchos especialistas en lugar de procedimientos quirúrgicos.
Biopsia abierta:
Consiste en realizar una incisión en la piel para acceder visualmente a la tiroides. Se recurre a este método cuando otras pruebas no han proporcionado una causa clara a los síntomas.
Biopsia con aguja gruesa:
Se introduce una aguja especial para extraer una muestra de tejido de tamaño similar al de un grano de arroz.
Los propósitos de la biopsia tiroidea abarca en identificar la causa de un bulto o nódulo detectado en la tiroides, ya sea durante un examen físico o a través de pruebas como la ecografía o la gammagrafía tiroidea y determinar la causa de un agrandamiento de la tiroides (bocio), caracterizado por problemas al tragar o respirar, sensación de hinchazón en el cuello y pérdida de peso.
Preparación para el procedimiento:
Antes de la biopsia, es importante informar al médico sobre:
- Cualquier medicación que se tome regularmente, incluyendo nombres y dosis.
- Alergias a medicamentos, especialmente a anestésicos.
- Uso de medicamentos para prevenir coágulos o historial de problemas de sangrado.
- Es posible que se realicen análisis de sangre para verificar problemas de coagulación antes de la biopsia tiroidea.
Pasos previos al procedimiento:
- Para una biopsia por punción, no se requiere ningún paso de preparación específico. El paciente estará despierto durante el procedimiento.
- En caso de una biopsia abierta, se administrará anestesia general y el paciente estará dormido. Se deben seguir las instrucciones precisas sobre el ayuno antes del procedimiento, y si se deben tomar medicamentos el día del mismo, hacerlo únicamente con un sorbo de agua.
- Antes de la prueba, es necesario retirar la dentadura postiza (si se usa) y cualquier joya u objeto metálico alrededor del cuello y la parte superior del cuerpo.
Desarrollo del procedimiento:
Se realiza en un hospital, clínica o consultorio médico. Durante el procedimiento, el paciente estará acostado con la cabeza inclinada hacia atrás y el cuello extendido para facilitar la biopsia. Es esencial evitar toser, hablar o tragar mientras la aguja esté en su lugar. La duración aproximada es de 5 a 10 minutos.
Antes de la biopsia, es posible que se administre un sedante para relajar al paciente. El médico limpiará la piel sobre la tiroides con un jabón especial.
El médico puede usar una ecografía para guiar la colocación de la aguja, extrayendo una pequeña cantidad de tejido y líquido tiroideos para su observación bajo el microscopio. Se coloca una pequeña venda en el lugar de la inserción de la aguja.
Biopsia abierta.
Realizada por un cirujano en un quirófano cuando otras pruebas no han identificado la causa de los síntomas. La duración es aproximadamente de una hora.
Es posible que se administre un sedante para relajar al paciente. Se coloca una vía intravenosa en el brazo para suministrar medicamentos y líquidos. El paciente estará dormido durante la biopsia.
La piel sobre la tiroides se limpia con un jabón especial. Se realiza una incisión en el cuello para tomar una muestra de tejido tiroideo o, en algunos casos, extirpar el bulto sospechoso. Parte del tejido puede ser enviado al laboratorio para examinar si hay células cancerosas. Si se detectan células cancerosas, el médico puede optar por extirpar una porción mayor o la totalidad de la tiroides.
La incisión se cierra con puntos de sutura y se coloca una venda sobre ellos. Se recomienda mantener el sitio de la biopsia cubierto y seco durante 48 horas. Es normal esperar un leve sangrado del sitio de la biopsia, por lo que es importante consultar al médico sobre la cantidad esperada. Algunas personas pueden necesitar permanecer en el hospital durante una noche.
El procedimiento de biopsia abierta no se realiza con tanta frecuencia como el de biopsia por punción.
Sensaciones durante y después del procedimiento:
Biopsia por punción.
Puede resultar incómodo permanecer inmóvil con la cabeza reclinada hacia atrás.
Durante la biopsia por punción, es posible sentir un rápido pinchazo en el cuello.
El sitio de la biopsia puede sentirse dolorido y sensible durante 1 o 2 días. Se pueden tomar analgésicos de venta libre, como el acetaminofén, para aliviar la molestia, siguiendo las indicaciones de la etiqueta.
Biopsia abierta.
El paciente estará dormido y no sentirá nada durante la biopsia. Es posible que después del procedimiento se experimenten náuseas, dolores musculares generales y fatiga durante 1 o 2 días. También puede haber dolor de garganta y ronquera. Para aliviar el dolor de garganta, se pueden chupar caramelos duros o hacer gárgaras con agua tibia y sal.
El sitio de la biopsia puede sentirse dolorido y sensible durante 3 o 4 días. El médico puede recetar analgésicos para esto.
Después de someterse a una biopsia tiroidea, es recomendable mantener la cabeza apoyada en una almohada al acostarse para mayor comodidad. Al levantarse, sostenga la parte posterior de su cabeza y cuello con ambas manos para evitar molestias en el lugar de la biopsia.
Riesgos asociados:
Existe una pequeña posibilidad de complicaciones derivadas de una biopsia tiroidea, como la posibilidad de infección o sangrado.
Posterior a la prueba:
Es crucial comunicarse con su médico de inmediato si experimenta:
- Sangrado considerable que traspasa el vendaje.
- Dificultades para tragar.
Indicios de infección, como:
- Aumento del dolor, inflamación, calor o enrojecimiento alrededor del área de la biopsia.
- Venas rojizas que se extienden desde el sitio de la biopsia.
- Secreción de pus desde el área de la biopsia.
- Aparición de ganglios linfáticos inflamados en el cuello.
- Presencia de fiebre.
Resultados de la biopsia tiroidea:
Normal: El tejido tiroideo analizado muestra un estado normal.
Anormal: La muestra revela una condición relacionada con la tiroides, como inflamación, cáncer o un tumor no canceroso (benigno). Se identifica un quiste tiroideo durante la biopsia. En su mayoría, los quistes de la tiroides no son cancerosos.